pH senken mit Salzsäure
Hier wird im Einzelnen meine Vorgehensweise beschrieben. Ziel ist es eine Schrittweise Erniedrigung des pH-Wertes zu erreichen. Ich weise darauf hin, dass ich mein Experiment ohne Fische durchgeführt habe. Das Becken befand sich während der pH-Wert Senkung in der Einlaufphase. Mit Säure wurde nur im Eimer gearbeitet, nicht im Aquarium. Nach Überprüfung des Wechselwassers wurde dieses dann ins Aquarium gegeben.
Theoretische Vorüberlegungen
In diesem Abschnitt geht es erstmal um theoretische Vorüberlegungen um die benötigten Mengen an Salzsäure abschätzen zu können.
Berechnung der ungefähren Wassermenge
Ich habe ein 54 l Becken von dem aber 2 cm an der oberen Kante nicht mit Wasser befüllt sind:
(60*30*2)/1000=3,6l
Berücksichtigt werden muss auch der Kies (1-3 mm Körnung) der bei mir eine durchschnittlich Höhe von 4cm hat. Ich gehe davon aus, dass sich 1l Wasser in den Zwischenräumen befindet. Wer Lust hat die genaue Schütt-Dichte des Kieses zu berücksichtigen, kann mir die Ergebnisse gerne schicken ... :-).
((60*30*4)/1000)-1=6,2l
Für Filter, Heizer, Wurzel und Biomasse setze ich nochmal 2l an, wir kommen damit auf ein Wasservolumen von:
54l - 3,6l - 6,2l - 2l = 42,2l naja, sagen wir 42l.
Berechnung der Masse an Hydrogencarbonat
Die Menge an Hydrogencarbonat-Ionen sind vom Wasserversorger vorgegeben. Bei mir sind dies 63 mg/l, damit ergibt sich:
![]()
Das bedeutet, dass ungefähr 2,646 g Hydrogencarbonat im Becken sind.
Die meisten Wasserversorger gebe das Säurebindungsvermögen (auch Säurekapazität genannt) an. Die Beziehugen zwischen dem Säurebindungsvermögen und der Karbonathärte lässt sich wie folgt definieren:
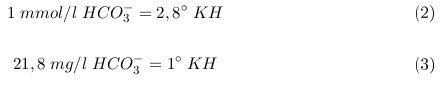
Berechnung der benötigten Menge Salzsäure
Die Dehydrokarbonisierung läuft nach folgender Gleichung ab:
![]()
Mit den Molekularmassen und unserer Menge an Hydrogencarbonat (1) ergibt sich:
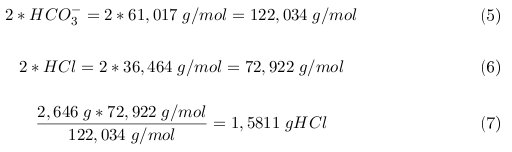
Das heisst, es werden 1,5811 g benötigt um das Hydrogencarbonat zu neutralisieren.
Verwendung einer 3% Salzsäure
Der nächste Schritt ist die Berechnung der Masse an HCl in einer 3% Salzsäure. Die Dichte beträgt 1,0131 g/ml. Das bedeutet, 1000 ml einer 3% HCl hat die Masse von 1013,1g. Damit ergibt sich die Menge an HCl pro ml:
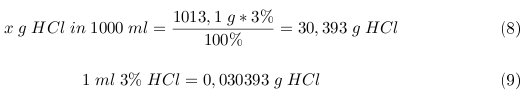
Aus Gleichung (7) ergibt sich dann das theoretische Volumen an 3% Salzsäure die für das Entfernen des Hydrogencarbonates im Becken erforderlich sind:
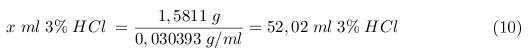
Für die Aufbereitung von 10l Wechselwassers ergibt sich damit eine Salzsäure Menge von:
![]()